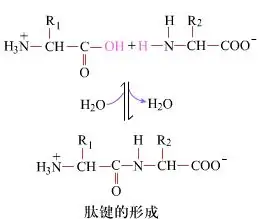
Oppervlakkig gezien is de vorming van peptidebindingen, die dipeptiden opleveren, een eenvoudig chemisch proces.Dit betekent dat de twee aminozuurcomponenten met elkaar verbonden zijn door een peptidebinding, een amidebinding, terwijl ze gedehydrateerd zijn.
De vorming van peptidebindingen is de activering van een aminozuur onder milde reactieomstandigheden.(A) carboxylgroep, tweede aminozuur (B) De nucleofiele geactiveerde carboxylgroep vormt vervolgens het dipeptide (AB).“Als de carboxylcomponent (A) niet wordt beschermd, kan de vorming van de peptidebinding niet worden gecontroleerd.”Bijproducten zoals lineaire en cyclische peptiden kunnen worden gemengd met doelverbindingen AB.Daarom moeten alle functionele groepen die niet betrokken zijn bij de vorming van peptidebindingen op een tijdelijk omkeerbare manier worden beschermd tijdens de peptidesynthese.
De peptidesynthese – de vorming van elke peptidebinding – omvat dus drie aggregatiestappen.
De eerste stap is het bereiden van enkele aminozuren die bescherming nodig hebben, en de zwitterionische structuur van aminozuren bestaat niet meer.
De tweede stap is een tweestapsreactie om peptidebindingen te vormen, waarbij de carboxylgroep van het N-beschermde aminozuur eerst wordt geactiveerd tot het actieve tussenproduct en vervolgens de peptidebinding wordt gevormd.Deze gekoppelde reactie kan plaatsvinden als een eenstapsreactie of als twee opeenvolgende reacties.
De derde stap is het selectief verwijderen of volledig verwijderen van de beschermende basis.Hoewel alle verwijdering pas kan plaatsvinden nadat alle peptideketens zijn samengesteld, is selectieve verwijdering van beschermende groepen ook vereist om de peptidesynthese voort te zetten.
Omdat 10 aminozuren (Ser, Thr, Tyr, Asp, Glu, Lys, Arg, His, Sec en Cys) functionele zijketengroepen bevatten, die selectieve bescherming vereisen, waardoor de peptidesynthese ingewikkelder wordt.Tijdelijke en semi-permanente beschermingsbases moeten worden onderscheiden vanwege de verschillende vereisten voor selectiviteit.Tijdelijke beschermingsgroepen worden in de volgende stap gebruikt om de tijdelijke bescherming van functionele aminozuur- of carboxylgroepen weer te geven.Semi-permanente beschermende groepen worden verwijderd zonder de reeds gevormde peptidebindingen of zijketens van aminozuren te verstoren, soms tijdens de synthese.
“In het ideale geval zou de activering van de carboxylcomponent en de daaropvolgende vorming van peptidebindingen (koppelingsreacties) snel moeten zijn, zonder racemische vorming of vorming van bijproducten, en zouden molaire reactanten moeten worden toegepast om hoge opbrengsten te bereiken.”Helaas voldoet geen van de chemische koppelingsmethoden aan deze eisen, en weinigen zijn geschikt voor praktische synthese.
Tijdens de peptidesynthese zijn de functionele groepen die betrokken zijn bij verschillende reacties meestal gekoppeld aan het handmatige centrum, waarbij glycine de enige uitzondering is, en er is een potentieel risico op rotatie.
De laatste stap in de peptidesynthesecyclus is de verwijdering van alle beschermende groepen.Selectieve verwijdering van beschermende groepen is belangrijk voor de verlenging van de peptideketen, naast de vereiste voor volledige verwijdering van bescherming bij dipeptidesynthese.Synthetische strategieën moeten zorgvuldig worden gepland.Afhankelijk van de strategische keuze kan N selectief de a-amino- of carboxyl-beschermende groepen verwijderen.De term ‘strategie’ verwijst naar de volgorde van condensatiereacties van individuele aminozuren.Over het algemeen is er een verschil tussen geleidelijke synthese en fragmentcondensatie.Peptidesynthese (ook bekend als “conventionele synthese”) vindt plaats in oplossing.In de meeste gevallen kan de geleidelijke verlenging van de peptideketen alleen worden gesynthetiseerd door de peptideketen te gebruiken om kortere fragmenten te synthetiseren.Om langere peptiden te synthetiseren, moeten de doelmoleculen in geschikte fragmenten worden gesegmenteerd en worden vastgesteld dat ze de mate van differentiatie aan het C-uiteinde kunnen minimaliseren.Nadat de individuele fragmenten geleidelijk zijn samengevoegd, zal de doelverbinding worden samengevoegd.De strategie van peptidesynthese omvat de selectie van het beste en meest geschikte beschermende fragment, en de strategie van peptidesynthese omvat de selectie van de meest geschikte combinatie van beschermende basen en de beste methode voor fragmentconjugatie.
Posttijd: 19 juli 2023