Peptiden zijn een klasse verbindingen die worden gevormd door de verbinding van meerdere aminozuren via peptidebindingen.Ze zijn alomtegenwoordig in levende organismen.Tot nu toe zijn er tienduizenden peptiden aangetroffen in levende organismen.Peptiden spelen een belangrijke rol bij het reguleren van de functionele activiteiten van verschillende systemen, organen, weefsels en cellen en bij levensactiviteiten, en worden vaak gebruikt bij functionele analyse, onderzoek naar antilichamen, de ontwikkeling van geneesmiddelen en andere gebieden.Met de ontwikkeling van biotechnologie en peptidesynthesetechnologie zijn steeds meer peptidegeneesmiddelen ontwikkeld en klinisch toegepast.
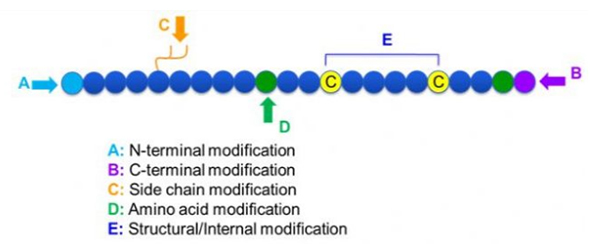
Er is een grote verscheidenheid aan peptidemodificaties, die eenvoudigweg kunnen worden onderverdeeld in postmodificatie en procesmodificatie (met behulp van afgeleide aminozuurmodificatie), en N-terminale modificatie, C-terminale modificatie, zijketenmodificatie, aminozuurmodificatie, skeletmodificatie, enz., afhankelijk van de wijzigingslocatie (Figuur 1).Als een belangrijk middel om de hoofdketenstructuur of zijketengroepen van peptideketens te veranderen, kan peptidemodificatie de fysische en chemische eigenschappen van peptideverbindingen effectief veranderen, de wateroplosbaarheid verhogen, de actietijd in vivo verlengen, hun biologische distributie veranderen, immunogeniciteit elimineren. , toxische bijwerkingen verminderen, enz. In dit artikel worden verschillende belangrijke strategieën voor peptidemodificatie en hun kenmerken geïntroduceerd.
1. Cyclisatie
Cyclische peptiden hebben veel toepassingen in de biogeneeskunde, en veel natuurlijke peptiden met biologische activiteit zijn cyclische peptiden.Omdat cyclische peptiden doorgaans stijver zijn dan lineaire peptiden, zijn ze extreem resistent tegen het spijsverteringsstelsel, kunnen ze overleven in het spijsverteringskanaal en vertonen ze een sterkere affiniteit voor doelreceptoren.Cyclisatie is de meest directe manier om cyclische peptiden te synthetiseren, vooral voor peptiden met een groot structureel skelet.Volgens de cyclisatiemodus kan het worden onderverdeeld in zijketen-zijketentype, terminal - zijketentype, terminal - terminaltype (end-to-end-type).
(1) zijketen-tot-zijketen
Het meest voorkomende type cyclisatie van zijketen naar zijketen is de disulfidebrug tussen cysteïneresiduen.Deze cyclisatie wordt geïntroduceerd doordat een paar cysteïneresiduen worden ontschermd en vervolgens worden geoxideerd om disulfidebindingen te vormen.Polycyclische synthese kan worden bereikt door selectieve verwijdering van sulfhydrylbeschermingsgroepen.Cyclisatie kan worden uitgevoerd in een post-dissociatie-oplosmiddel of op een pre-dissociatiehars.Cyclisatie op harsen kan minder effectief zijn dan cyclisatie met oplosmiddel, omdat de peptiden op harsen niet gemakkelijk gecycliseerde conformaties vormen.Een ander type zijketen-zijketencyclisatie is de vorming van een amidestructuur tussen een asparaginezuur- of glutaminezuurresidu en het basisaminozuur, wat vereist dat de zijketenbeschermingsgroep selectief uit het polypeptide moet kunnen worden verwijderd. op de hars of na dissociatie.Het derde type zijketen-zijketencyclisatie is de vorming van difenylethers door tyrosine of p-hydroxyfenylglycine.Dit type cyclisatie in natuurlijke producten wordt alleen aangetroffen in microbiële producten, en cyclisatieproducten hebben vaak een potentiële medicinale waarde.De bereiding van deze verbindingen vereist unieke reactieomstandigheden, daarom worden ze niet vaak gebruikt bij de synthese van conventionele peptiden.
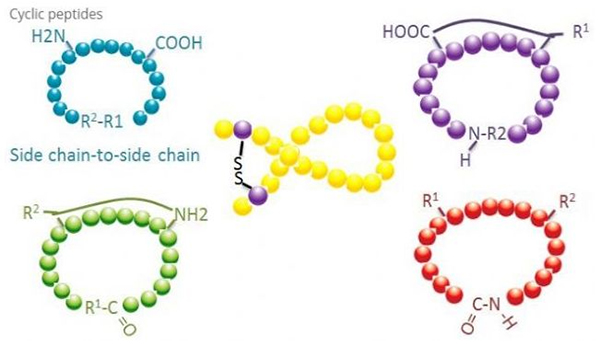
(2) terminal-naar-zijketen
Bij cyclisatie van de terminale zijketen is gewoonlijk het C-uiteinde betrokken met de aminogroep van de lysine- of ornithine-zijketen, of het N-uiteinde met de asparaginezuur- of glutaminezuurzijketen.Andere polypeptidecyclisatie wordt uitgevoerd door etherbindingen te vormen tussen terminale C- en serine- of threoninezijketens.
(3) Terminal- of kop-staart-type
Ketenpolypeptiden kunnen ofwel in een oplosmiddel worden gecirculeerd of op een hars worden gefixeerd door middel van zijketencycli.Bij de centralisatie van oplosmiddelen moeten lage concentraties peptiden worden gebruikt om oligomerisatie van peptiden te voorkomen.De opbrengst van een kop-tot-staart synthetisch ringpolypeptide hangt af van de sequentie van het ketenpolypeptide.Voordat cyclische peptiden op grote schaal worden bereid, moet daarom eerst een bibliotheek van mogelijke geketende leadpeptiden worden gecreëerd, gevolgd door cyclisatie om de sequentie met de beste resultaten te vinden.
2. N-methylering
N-methylering komt oorspronkelijk voor in natuurlijke peptiden en wordt geïntroduceerd in de peptidesynthese om de vorming van waterstofbruggen te voorkomen, waardoor peptiden beter bestand zijn tegen biologische afbraak en klaring.Synthese van peptiden met behulp van N-gemethyleerde aminozuurderivaten is de belangrijkste methode.Bovendien kan ook een Mitsunobu-reactie van N-(2-nitrobenzeensulfonylchloride)-polypeptide-harstussenproducten met methanol worden gebruikt.Deze methode is gebruikt om cyclische peptidebibliotheken te bereiden die N-gemethyleerde aminozuren bevatten.
3. Fosforylering
Fosforylatie is een van de meest voorkomende post-translationele modificaties in de natuur.In menselijke cellen is meer dan 30% van de eiwitten gefosforyleerd.Fosforylatie, vooral omkeerbare fosforylering, speelt een belangrijke rol bij het beheersen van veel cellulaire processen, zoals signaaltransductie, genexpressie, celcyclus- en cytoskeletregulatie, en apoptose.
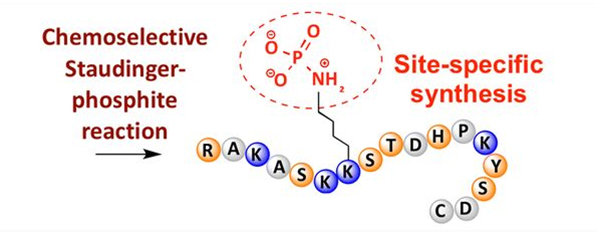
Fosforylatie kan worden waargenomen bij een verscheidenheid aan aminozuurresiduen, maar de meest voorkomende fosforyleringsdoelen zijn serine-, threonine- en tyrosineresiduen.Fosfotyrosine-, fosfothreonine- en fosfoserinederivaten kunnen tijdens de synthese in peptiden worden geïntroduceerd of na de peptidesynthese worden gevormd.Selectieve fosforylering kan worden bereikt met behulp van residuen van serine, threonine en tyrosine die selectief beschermende groepen verwijderen.Sommige fosforyleringsreagentia kunnen ook fosforzuurgroepen in het polypeptide introduceren door middel van postmodificatie.De afgelopen jaren is plaatsspecifieke fosforylering van lysine bereikt met behulp van een chemisch selectieve Staudinger-fosfietreactie (Figuur 3).
4. Myristoylatie en palmitoylatie
Acylatie van het N-uiteinde met vetzuren zorgt ervoor dat peptiden of eiwitten aan celmembranen kunnen binden.De gemyridamoyleerde sequentie op het N-uiteinde maakt het mogelijk dat Src-familie-eiwitkinasen en reverse-transcriptase Gaq-eiwitten doelgericht kunnen binden aan celmembranen.Myristinezuur werd gekoppeld aan het N-uiteinde van het hars-polypeptide met behulp van standaard koppelingsreacties, en het resulterende lipopeptide kon onder standaardomstandigheden worden gedissocieerd en gezuiverd door RP-HPLC.
5. Glycosylering
Glycopeptiden zoals vancomycine en teicolanine zijn belangrijke antibiotica voor de behandeling van geneesmiddelresistente bacteriële infecties, en andere glycopeptiden worden vaak gebruikt om het immuunsysteem te stimuleren.Omdat veel microbiële antigenen geglycosyleerd zijn, is het bovendien van groot belang om glycopeptiden te bestuderen voor het verbeteren van het therapeutische effect van infectie.Aan de andere kant is gevonden dat de eiwitten op het celmembraan van tumorcellen abnormale glycosylatie vertonen, waardoor glycopeptiden een belangrijke rol spelen bij onderzoek naar kanker en de immuunafweer van tumoren.Glycopeptiden worden bereid volgens de Fmoc/t-Bu-methode.Geglycosyleerde residuen, zoals threonine en serine, worden vaak in polypeptiden geïntroduceerd door door pentafluorfenolester geactiveerde fMOC's om geglycosyleerde aminozuren te beschermen.
6. Isopreen
Isopentadienylering vindt plaats op cysteïneresiduen in de zijketen nabij het C-uiteinde.Eiwitisopreen kan de celmembraanaffiniteit verbeteren en eiwit-eiwitinteractie vormen.Geïsopentadieneerde eiwitten omvatten tyrosinefosfatase, kleine GTase, cochaperonmoleculen, nucleaire lamina en centromere bindende eiwitten.Isopreenpolypeptiden kunnen worden bereid met behulp van isopreen op harsen of door cysteïnederivaten te introduceren.
7. Modificatie van polyethyleenglycol (PEG).
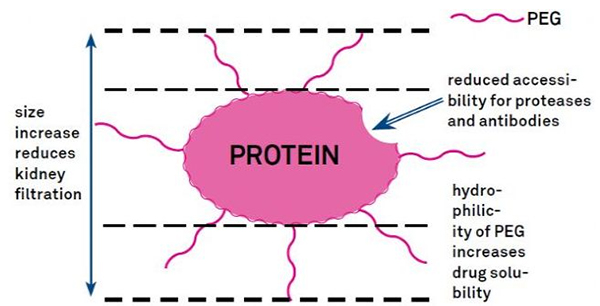
PEG-modificatie kan worden gebruikt om de hydrolytische stabiliteit van eiwitten, de biodistributie en de oplosbaarheid van peptiden te verbeteren.De introductie van PEG-ketens in peptiden kan hun farmacologische eigenschappen verbeteren en ook de hydrolyse van peptiden door proteolytische enzymen remmen.PEG-peptiden passeren gemakkelijker de glomerulaire capillaire dwarsdoorsnede dan gewone peptiden, waardoor de renale klaring aanzienlijk wordt verminderd.Vanwege de verlengde actieve halfwaardetijd van PEG-peptiden in vivo kan het normale behandelingsniveau worden gehandhaafd met lagere doses en minder frequente peptidegeneesmiddelen.PEG-modificatie heeft echter ook negatieve effecten.Grote hoeveelheden PEG voorkomen dat het enzym het peptide afbreekt en verminderen ook de binding van het peptide aan de doelreceptor.Maar de lage affiniteit van PEG-peptiden wordt meestal gecompenseerd door hun langere farmacokinetische halfwaardetijd, en doordat ze langer in het lichaam aanwezig zijn, hebben PEG-peptiden een grotere kans om in doelweefsels te worden geabsorbeerd.Daarom moeten de PEG-polymeerspecificaties worden geoptimaliseerd voor optimale resultaten.Aan de andere kant hopen PEG-peptiden zich op in de lever als gevolg van verminderde renale klaring, resulterend in macromoleculair syndroom.Daarom moeten PEG-modificaties zorgvuldiger worden ontworpen wanneer peptiden worden gebruikt voor het testen van geneesmiddelen.
Veel voorkomende modificatiegroepen van PEG-modificatoren kunnen grofweg als volgt worden samengevat: Amino (-amine) -NH2, aminomethyl-Ch2-NH2, hydroxy-OH, carboxy-Cooh, sulfhydryl (-Thiol) -SH, Maleimide -MAL, succinimidecarbonaat - SC, succinimide-acetaat -SCM, succinimidepropionaat -SPA, n-hydroxysuccinimide -NHS, acrylaat-ch2ch2cooh, aldehyde -CHO (zoals propional-ald, butyrALD), acrylbasis (-acrylaat-acrl), azido-azide, biotinyl - Biotine, fluoresceïne, glutaryl -GA, acrylaathydrazide, alkyn-alkyn, p-tolueensulfonaat -OT's, succinimidesuccinaat -SS, enz. PEG-derivaten met carbonzuren kunnen worden gekoppeld aan n-terminale aminen of lysinezijketens.Amino-geactiveerd PEG kan worden gekoppeld aan zijketens van asparaginezuur of glutaminezuur.Mal-geactiveerd PEG kan worden geconjugeerd aan mercaptan van volledig ontschermde cysteïnezijketens [11].PEG-modificatoren worden gewoonlijk als volgt geclassificeerd (let op: mPEG is methoxy-PEG, CH3O-(CH2CH2O)n-CH2CH2-OH):
(1) PEG-modificator met rechte keten
mPEG-SC, mPEG-SCM, mPEG-SPA, mPEG-OT's, mPEG-SH, mPEG-ALD, mPEG-butyRALD, mPEG-SS
(2) bifunctionele PEG-modificator
HCOO-PEG-COOH, NH2-PEG-NH2, OH-PEG-COOH, OH-PEG-NH2, HCl·NH2-PEG-COOH, MAL-PEG-NHS
(3) vertakkende PEG-modificator
(mPEG)2-NHS, (mPEG)2-ALD, (mPEG)2-NH2, (mPEG)2-MAL
8. Biotinisatie
Biotine kan sterk gebonden worden met avidine of streptavidine, en de bindingssterkte ligt zelfs dicht bij een covalente binding.Met biotine gemerkte peptiden worden vaak gebruikt in immunoassay, histocytochemie en op fluorescentie gebaseerde flowcytometrie.Gelabelde antibiotine-antilichamen kunnen ook worden gebruikt om gebiotinyleerde peptiden te binden.Biotinelabels worden vaak bevestigd aan de lysinezijketen of het N-uiteinde.6-aminocapronzuur wordt vaak gebruikt als binding tussen peptiden en biotine.De binding is flexibel in binding aan het substraat en bindt beter in aanwezigheid van sterische hindering.
9. Fluorescerende etikettering
Fluorescerende labeling kan worden gebruikt om polypeptiden in levende cellen te traceren en om enzymen en werkingsmechanismen te bestuderen.Tryptofaan (Trp) is fluorescerend en kan dus worden gebruikt voor intrinsieke labeling.Het emissiespectrum van tryptofaan hangt af van de perifere omgeving en neemt af naarmate de polariteit van het oplosmiddel afneemt, een eigenschap die nuttig is voor het detecteren van de peptidestructuur en receptorbinding.Tryptofaanfluorescentie kan worden gedoofd door geprotoneerd asparaginezuur en glutaminezuur, wat het gebruik ervan kan beperken.De Dansylchloridegroep (Dansyl) is sterk fluorescerend wanneer gebonden aan een aminogroep en wordt vaak gebruikt als fluorescerend label voor aminozuren of eiwitten.
Fluorescentie-resonantie Energieconversie (FRET) is nuttig voor enzymstudies.Wanneer FRET wordt toegepast, bevat het substraatpolypeptide gewoonlijk een fluorescentielabelende groep en een fluorescentiedovende groep.Gelabelde fluorescerende groepen worden door de quencher gedoofd door middel van niet-foton-energieoverdracht.Wanneer het peptide wordt gedissocieerd van het betreffende enzym, zendt de labelende groep fluorescentie uit.
10. Kooipolypeptiden
Kooipeptiden hebben optisch verwijderbare beschermende groepen die het peptide beschermen tegen binding aan de receptor.Bij blootstelling aan UV-straling wordt het peptide geactiveerd, waardoor de affiniteit voor de receptor wordt hersteld.Omdat deze optische activering kan worden geregeld op basis van tijd, amplitude of locatie, kunnen kooipeptiden worden gebruikt om reacties die in cellen optreden te bestuderen.De meest gebruikte beschermende groepen voor kooipolypeptiden zijn 2-nitrobenzylgroepen en hun derivaten, die via beschermende aminozuurderivaten in de peptidesynthese kunnen worden geïntroduceerd.Aminozuurderivaten die zijn ontwikkeld zijn lysine, cysteïne, serine en tyrosine.Aspartaat- en glutamaatderivaten worden echter niet vaak gebruikt vanwege hun gevoeligheid voor cyclisatie tijdens peptidesynthese en dissociatie.
11. Polyantigeen peptide (MAP)
Korte peptiden zijn meestal niet immuun en moeten aan dragereiwitten worden gekoppeld om antilichamen te produceren.Polyantigeen peptide (MAP) is samengesteld uit meerdere identieke peptiden verbonden met lysinekernen, die specifiek immunogenen met hoge potentie tot expressie kunnen brengen en kunnen worden gebruikt om peptide-dragereiwitkoppelingen te bereiden.MAP-polypeptiden kunnen worden gesynthetiseerd door vaste fase-synthese op MAP-hars.Onvolledige koppeling resulteert echter in ontbrekende of ingekorte peptideketens op sommige takken en vertoont dus niet de eigenschappen van het oorspronkelijke MAP-polypeptide.Als alternatief kunnen peptiden afzonderlijk worden bereid en gezuiverd en vervolgens aan MAP worden gekoppeld.De peptidesequentie die aan de peptidekern is bevestigd, is goed gedefinieerd en gemakkelijk gekarakteriseerd door massaspectrometrie.
Conclusie
Peptidemodificatie is een belangrijk middel om peptiden te ontwerpen.Chemisch gemodificeerde peptiden kunnen niet alleen een hoge biologische activiteit behouden, maar ook effectief de nadelen van immunogeniciteit en toxiciteit vermijden.Tegelijkertijd kan chemische modificatie peptiden een aantal nieuwe uitstekende eigenschappen geven.De afgelopen jaren is de methode van CH-activering voor de post-modificatie van polypeptiden snel ontwikkeld en zijn er veel belangrijke resultaten bereikt.
Posttijd: 20 maart 2023
